3. I Zasada termodynamiki, bilans energii i stany skupienia
I zasada termodynamiki
Zmiana energii wewnętrznej układu jest równa sumie ciepła dostarczonego do układu i pracy wykonanej nad układem.
ΔU = Q + W
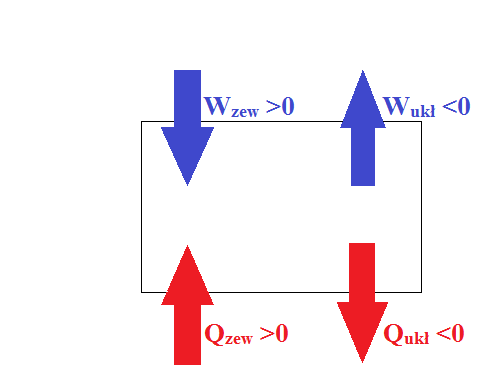
Qzew = -Qukł
Wzew = -Wukł
Równoważność ciepła i pracy:
Energię wewnętrzną ciała można zmienić zarówno dostarczając ciepła, jak i wykonując pracę.
Bilans cieplny
W sytuacji wymiany ciepła przez dwa ciała, w następstwie zasady zachowania energii, ciepło oddane przez jedno ciało jest równe ciepłu pobranemu przez drugie ciało.
Qoddane = Qpobrane
Stany skupienia mikroskopowo:
- gazowy – cząsteczki są oddalone od siebie, poruszają się, substancja nie zachowuje objętości i kształtu, przyjmuje objętość i kształt naczynia, zajmuje całą dostępną przestrzeń
- ciekły – cząsteczki są bliżej siebie, poruszają się, substancja zachowuje objętość, ale nie zachowuje kształtu
- stały – cząsteczki są bardzo blisko siebie, ciało zachowuje kształt i objętość, większość ma budowę krystaliczną, czyli cząsteczki są równo rozłożone tworząc uporządkowaną, powtarzającą się w trzech wymiarach strukturę

 (495 votes, average: 4,24 out of 5)
(495 votes, average: 4,24 out of 5)